Radikálová substituce (SR)
Při radikálové substituci dochází k nahrazení (substituci) vodíku za radikál jiného prvku či skupinu atomů. Probíhá za vyšších teplot nebo vlivem UV záření, aby mohlo dojít k homolytickému zániku vazeb.
Výsledkem těchto reakcí je směs různých produktů.
V praxi nejčastěji prováděné radikálové substituce alkanů jsou halogenace, nitrace, sulfochlorace a oxidace.
A) Halogenace
Halogenací dochází k náhradě jednoho nebo více vodíkových atomů (podle podmínek, za kterých reakce probíhá) v molekulách alkanů atomy halogenů. Produkty halogenace jsou halogenderiváty alkanů. Aktivační energie nutná k vyvolání (= zahájení) reakce se reaktantům dodává buď v podobě ultrafialového záření, nebo tepla (k zahájení halogenace je zapotřebí dosáhnout teploty 250–400 °C).
Reaktivita halogenů k alkanům klesá v řadě: F > Cl > Br > I. Tato reakce je v praxi proveditelná pouze pro chlor a brom. Fluorace je totiž natolik exotermní, že ji bez speciálních opatření nelze provést. Jodace je také prakticky neproveditelná, důvody pro to jsou ale opačné. První a rozhodující krok jodace je silně endotermní, a použijeme-li takové reakční podmínky, aby přesto probíhala, produkty jsou již za těchto podmínek nestabilní.
Mechanismus radikálové halogenace alkanů vysvětlíme na příkladu chlorace methanu, která má největší praktický význam.
Radikálová substituce má z hlediska reakčního mechanismu poměrně složitý průběh. Lze ji rozdělit do tří po sobě následujících fází: zahájení (= iniciace), šíření (= propagace) a zakončení (= terminace).
1) iniciace = zahájení
V této fázi dochází k homolytickému rozštěpení chemické vazby v molekule halogenu - chloru (halogen v reakci vystupuje jako činidlo, alkan je substrát) působením energie ultrafialového záření nebo tepla za vzniku dvou radikálů chloru:

2) propagace = šíření
V této fázi reakce narazí jeden ze dvou vzniklých radikálů chloru do molekuly methanu a způsobí homolýzu vazby mezi atomem uhlíku a vodíku. Výsledkem je alkylový (methylový) radikál a molekula chlorovodíku. Methylový radikál ihned napadá další nedisociované molekuly chloru a vzniká chlormethan a chlorový radikál. Chlorový radikál opět vstupuje do reakce, takže na jeden iniciační krok proběhne velké množství propagačních cyklů. Říkáme, že jde o řetězovou reakci.
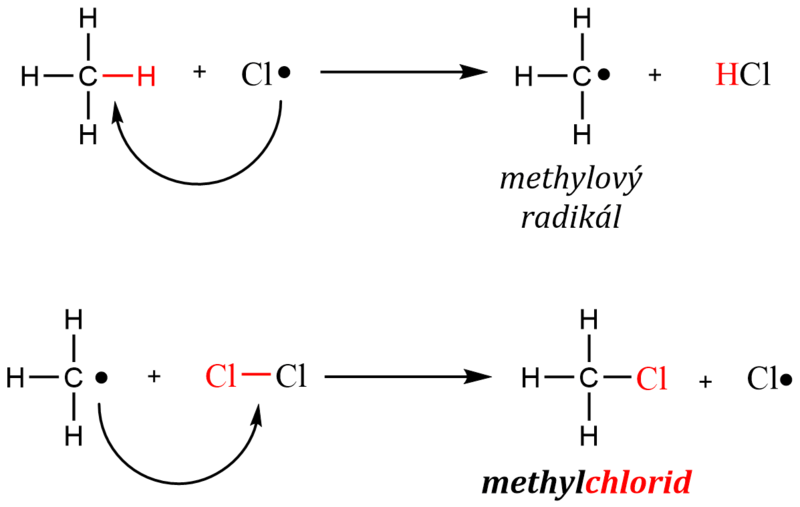
3) terminace = zakončení
Celá reakce je zakončena sloučením zbylých radikálů v reakční směsi:
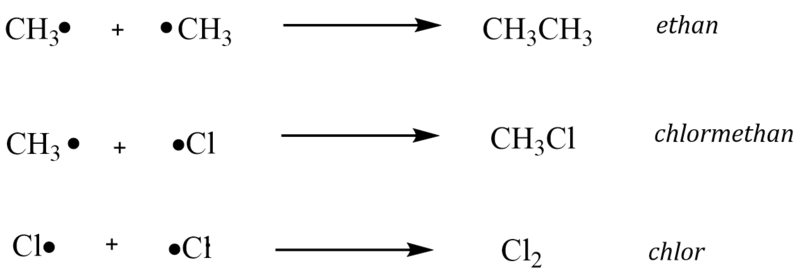
Obsahuje-li alkylový radikál atom vodíku vázaný na atomu uhlíku sousedící s uhlíkem nesoucím nepárový elektron, může dojít k eliminaci vodíkového radikálu a vzniku nenasyceného uhlovodíku. Příkladem může být eliminace vodíkového radikálu z ethylového radikálu.

Souhrnně lze chloraci methanu zapsat chemickou rovnicí:
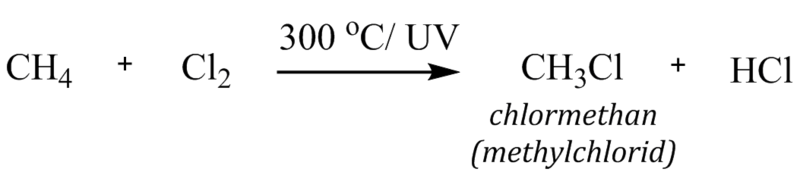
Všechny tyto kroky jsou zapsány pro chloraci methanu do prvního stupně. Produktem reakce je chlormethan. Ten má ještě další tři atomy vodíku, které rovněž mohou být nahrazeny chlorem za vzniku dichlormethanu, trichlormethanu, až tetrachlormethanu.
Z uvedeného tedy plyne, že chlorace methanu probíhá až do čtvrtého stupně. Ke vzniku této směsi dochází vždy i při použití poměru 1 molu alkanu na jeden mol halogenu. Poměr jednotlivých produktů lze do jisté míry ovlivnit volbou poměru alkan : halogen. Vzniklá směs produktů se dělí destilačně.
Celkový průběh reakce při nadbytku chloru:
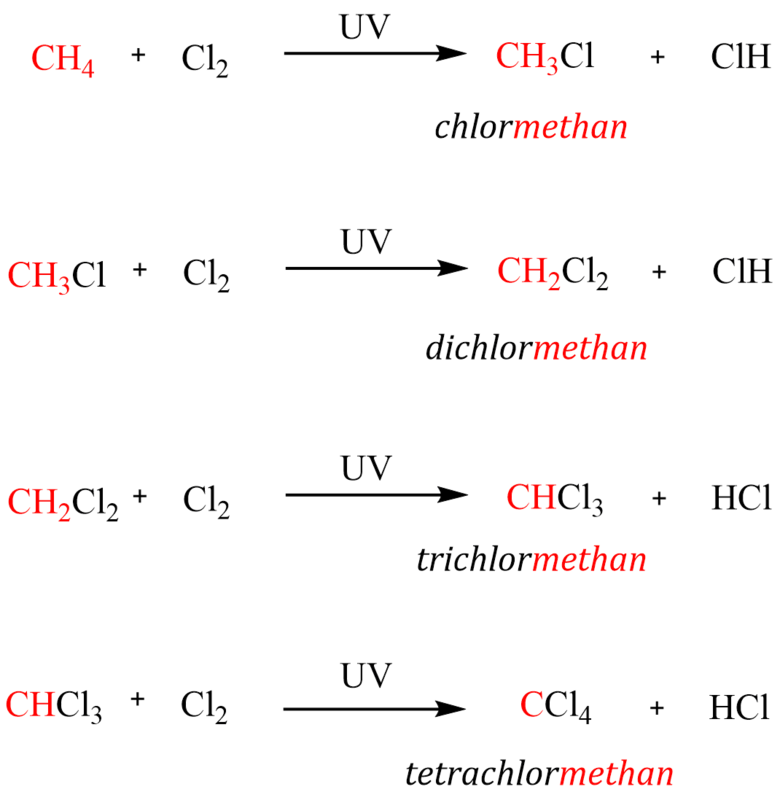
Chlorace vyšších alkanů je podobná jako u methanu, jen směs produktů je pestřejší. Chlorace ethanu do prvního stupně vede ke vzniku chlorethanu, který může podléhat další chloraci za vzniku dvou různých dihalogenderivátů (1,1 – dichlorethanu a 1,2 – dichlorethanu):
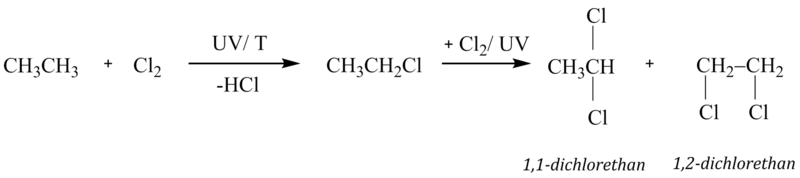
V případě propanu se v molekule nachází dva uhlíkové atomy methylových skupin nesoucí tři atomy vodíku, nazývané primární a jeden uhlíkový atom methylenové skupiny nesoucí dva atomy vodíku, nazývané sekundární. Proto při chloraci do prvního stupně musíme očekávat už dva různé monochlorderiváty (1–chlorpropan, 2–chlorpropan):
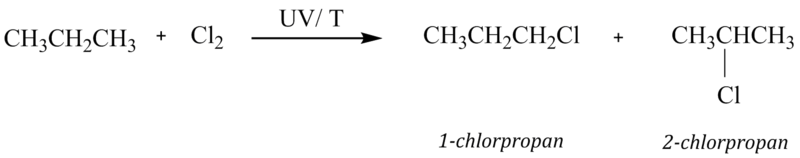
Z této a mnoha dalších reakcí vyplynulo, že nejlépe probíhá radikálová chlorace na terciárním uhlíku, hůře na sekundárním, potom primárním a nejhůře u methanu.
Závisí to na stabilitě vznikajícího radikálu, kdy nejstabilnější jsou terciární radikály, u nichž je nepárový elektron stabilizován kladným indukčním efektem tří alkylových substituentů, a tím dochází ke zvýšení stability systému.

B) Sulfochlorace
Sulfochlorací dochází k náhradě vodíku sulfochloridovou skupinou –SO2Cl.
Při této reakci se alkany nechají reagovat se sulfurylchloridem (SO2Cl2), ale častěji se směsí oxidu siřičitého a chloru.
Využívá se schopnosti alkylového radikálu reagovat s neutrální molekulou za vzniku složitějšího radikálu – alkansulfonylového, který je základem pro syntézu složitějších sloučenin. Iniciátorem reakce je opět UV záření.
Jako příklad si uvedeme sulfochloraci methanu:

Mechanismus sulfochlorace je téměř totožný s mechanismem chlorace alkanů, pouze přibývají další propagační kroky.
Zásadní pro pochopení průběhu této reakce je stabilita methansulfonylového volného radikálu, který vzniká interakcí methylového radikálu s oxidem siřičitým. Dvě násobné vazby S=O výrazným způsobem tento radikál stabilizují. Reakce s molekulou chloru proběhne až následně a produktem je chlorid methansulfonové kyseliny (methylsulfonylchlorid).

Alkany s dlouhým řetězcem poskytují alkansulfonylchloridy, z nichž zásaditou hydrolýzou vznikají soli alkansulfonových kyselin (alkyl-sulfonáty), které slouží jako detergenty.
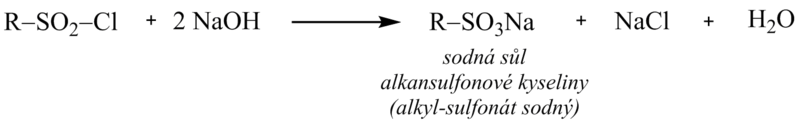
C) Nitrace
Nitrací dochází k náhradě vodíku nitroskupinou –NO2 .
K nitraci se používají oxidy dusíku (N2O5) nebo zředěná kyselina dusičná.
Při radikálové nitraci je průběh reakce složitější v závislosti na činidle i podmínkách reakce. V praxi se provádí nitrace nižších alkanů, nejčastěji methanu, jehož nitrací se získává nitromethan, který se používá jako rozpouštědlo i palivo do speciálních spalovacích motorů.
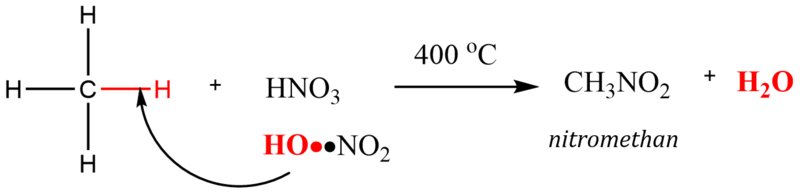
D) Oxidace
U alkanů má význam oxidace vzdušným kyslíkem, který s alkany reaguje jako biradikál kyslíku.
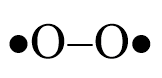
Podle rychlosti průběhu a možnosti zachycení jednotlivých meziproduktů oxidace lze oxidaci rozdělit na katalytickou (kontrolovanou) a hoření (popř. explozi).
Katalytická oxidace probíhá pomalu a jejími produkty jsou kyslíkaté deriváty, vznikající zpravidla v pořadí:
alkan → alkohol → karbonylová sloučenina → karboxylová kyselina → oxid uhličitý a voda
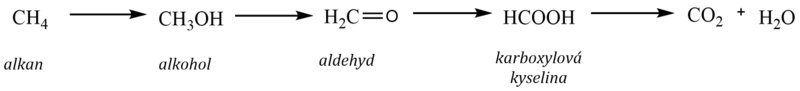
Kontrolovatelnost katalytické oxidace spočívá v tom, že reakci lze ukončit ve fázi vzniku požadovaného produktu. Tak lze laboratorně i průmyslově získat alkoholy, karbonylové i karboxylové sloučeniny.
Hoření alkanů probíhá velmi rychle až explozivně. Produktem hoření (za předpokladu dostatečného přístupu kyslíku) jsou oxid uhličitý a voda, jedná se o úplnou oxidaci alkanů. Silně exotermický charakter reakce umožňuje využití plynných alkanů a směsí kapalných alkanů při vytápění apod.

Při neúplné (nedokonalé) oxidaci vzniká uhlík (saze) a velmi toxický oxid uhelnatý. Jako příklad si můžeme uvést oxidaci propanu, který za dostatečného přístupu kyslíku oxiduje na oxid uhličitý a vodu, při menším množství kyslíku vzniká oxid uhelnatý a při nedostatku kyslíku se propan oxiduje na saze a vodu.

Vzhledem k ohromnému rozsahu využití spalování uhlovodíků dochází na naší planetě ke stále většímu hromadění oxidu uhličitého v atmosféře, což má za následek vznik skleníkového efektu.
Zdroje
- FIKR, Jaroslav a Jaroslav KAHOVEC. Názvosloví organické chemie. Olomouc: Rubico, 2002, ISBN 80-7346-017-3.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 2. díl. Olomouc: Nakladatelství Olomouc, 2005, ISBN 80-7182-141-1.
- JANECZKOVÁ, Anna a Pavel KLOUDA. Organická chemie. Ostrava: Nakladatelství Pavel Klouda, 1998, ISBN 80-902155-6-4/9802.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- PACÁK, Josef. Jak porozumět organické chemii. Praha: Karolinum, 1997, ISBN 80-7184-261-3.
- SVOBODA, Jiří a kol. Organická chemie I. Praha: Vysoká škola chemicko-technologická, 2005, ISBN 80-7080-561-7.
Obrázky
- Obr. 1: Autor neznámý. www.infovek.sk [online]. [cit. 24.10.2014]. Dostupný na WWW: http://www.infovek.sk/predmety/chemia/externe/majka/mydlostruktura.gif
- Obr. 2: Autor neznámý. www.hedvabnastezka.cz [online]. [cit. 24.10.2014]. Dostupný na WWW: http://www.hedvabnastezka.cz/public/data/uploads/svetoutdooru_cz/clanky/markillphoenix_10.jpg
- Obr. 3: Autor neznámý. www.alarmsecurity.cz [online]. [cit. 29.10.2014]. Dostupný na WWW: http://www.alarmsecurity.cz/fotky29870/CO.jpg
- Obr. 4: Autor neznámý. webmium.blob.core.windows.net [online]. [cit. 30.10.2014]. Dostupný na WWW: http://webmium.blob.core.windows.net/users/91706/assets/e980d140096c20325d48f286aadc7192/priznakyotravy.png
- Obr. 5: Autor neznámý. www.e-tabulky.cz [online]. [cit. 24.10.2014]. Dostupný na WWW: http://www.e-tabulky.cz/inshop/catalogue/products/pictures/1385S-105x105_V.jpg
- Obr. 6: Autor neznámý. www.nejlevnejsikrby.cz [online]. [cit. 24.10.2014]. Dostupný na WWW: http://www.nejlevnejsikrby.cz/_obchody/krby/prilohy/6/detektor-co-safe-0242-merici-zarizeni-0.jpg.big.jpg
Pokud není uvedeno jinak, autorem obrázků je Mgr. Michal Bezděk.
Čti také
Substituce
Substituce je chemická reakce, při které je atom nebo funkční skupina v molekule nahrazena za jiným atomem nebo skupinou.
Radikál
Částice s nepárovým elektronem.
Čti také
Substrát
Výchozí látka, která v průběhu reakce podléhá změnám.
Činidlo
Výchozí látka, která reaguje s různými substráty vždy stejným způsobem.
Čti také
Primární uhlík – vychází z něj jediná vazba k jinému uhlíkovému atomu.

Sekundární uhlík – vychází z něj dvě vazby na jiné uhlíkové atomy.

Terciární uhlík – vychází z něj tři vazby na jiné uhlíkové atomy.

Čti také
Kladný indukční efekt (+I efekt)
Tento efekt vyvolávají atomy a skupiny atomů, které mají nízkou elektronegativitu (alkyly) nebo sníženou elektronegativitu vlivem záporného náboje, např. –O–. Tyto atomy a skupiny atomů způsobují posun σ-elektronů na vazbách směrem od sebe a označují se jako elektrodonorní.

Odkaz
Bromace ethanu (mechanismus) - video
Zamysli se
Vedlejší produkty při halogenaci
I vznikající dichlorethany obsahují vazby C-H, a podléhají tak další chloraci. Kolik možných trichlorderivátů může vznikat? Napiš jejich vzorce.
Zamysli se
Kolik je v molekule 2-methylbutanu primárních, sekundárních a terciárních uhlíků?
Čti také
Detergenty
Detergenty jsou prací a čisticí prostředky sloužící k odstranění nečistot hlavně nepolárního charakteru, tj. mastného původu. Jejich molekula je složena z hydrofobních a hydrofilních skupin, které snižující povrchové napětí vody. Řadíme sem mýdla, prostředky na mytí nádobí, praní prádla nebo čištění předmětů.

Obr. 1: Stavba mýdla - hydrofilní a hydrofobní část
Jak fungují detergenty?
Složení moderních pracích prostředků

Procvič si
Reaktivita alkanů - viz přílohy
Čti také
Hoření
Hoření je proces, při němž oxidace látky probíhá rychle a silně exotermicky, za vývoje světla a tepla. K procesu hoření je obvykle zapotřebí všech tří složek: hořlavé látky, oxidačního činidla a zdroje zapálení. Nejčastějším oxidačním činidlem je vzdušný kyslík, existují ale i bezkyslíkaté oxidační prostředky, jako např. chlor. Zdrojem zapálení je nejčastěji plamen, jiskra nebo blesk.

Obr. 2: Hoření
Čti také
Oxid uhelnatý
Silně jedovatý plyn, který vzniká při nedokonalém spalování paliv. Je bezbarvý, bez chuti a bez zápachu, a proto je velmi obtížně zjistitelný lidskými smysly. Oxid uhelnatý se vdechováním váže na červené krevní barvivo hemoglobin (vzniká karbonylhemoglobin) asi 220krát lépe než kyslík. Stačí velmi malá koncentrace oxidu uhelnatého, aby zablokoval schopnost krve vázat a přenášet kyslík. CO je obsažen také v cigaretovém kouři!

Obr. 3: Pozor CO!
Nebezpečí oxidu uhelnatého - video
Zapamatuj si
Příznaky otravy CO
Prvními příznaky otravy CO jsou obvykle bolest hlavy a nevolnost.

Obr. 4: Příznaky otravy CO
Obr. 5: Symbol první pomoci
První pomoc
Vyvětrat, vynést postiženého ven, hlídat vědomí a dýchání, okamžité volat lékaře!
Prevence - detektor CO

Obr. 6: Detektor CO
Instalace detektoru CO - video





