Charakteristika
Alkeny jsou nenasycené acyklické uhlovodíky s jednou dvojnou vazbou. Dvojná vazba se skládá z jedné vazby σ a jedné vazby π. Uhlíkové atomy, ze kterých vychází dvojná vazba, jsou v hybridním stavu sp2 a jsou uspořádány v rovině. Vlivem dvojné vazby se mění valenční úhel ze 109°28’ na 120° a současně se zkracuje vzdálenost mezi oběma jádry a zvyšuje disociační energie vazby (pevnost).
Podle vzrůstajícího počtu uhlíkových atomů lze alkeny sestavit do homologické řady s homologickým rozdílem CH2 a homologickým vzorcem CnH2n.
Pro alkeny se dříve používalo označení olefiny, které pochází ze spojení latinských slov oleum (= ropa) a affinis (= slučivý). Důvodem byla jejich výroba z ropy.
Názvosloví
Systematické názvosloví alkenů se tvoří podobně jako názvosloví alkanů. Oproti nim se zde navíc objevuje dvojná vazba, jejíž přítomnost vyjadřujeme koncovkou –en, připojenou k základu názvu.
Při odvozování názvů alkenů vyhledáme hlavní řetězec, což je nejdelší souvislý uhlíkatý řetězec s největším počtem dvojných vazeb (násobných vazeb). Hlavní řetězec číslujeme tak, aby atom uhlíku, ze kterého dvojná vazba vychází, měl co nejnižší lokant (obecně polohy násobných vazeb musí být vyjádřeny co nejmenšími lokanty). Lokant násobné vazby vyjadřuje číslo atomu uhlíku, ze které vychází násobná vazba, v tomto případě dvojná.
Pokud se v řetězci nachází kromě dvojné vazby ještě substituent (např. methyl), má přednost při číslování dvojná vazba. Názvy substituentů umístíme v abecedním pořadí před základ názvu, včetně násobících předpon a lokantů, udávajících jejich polohu. Násobící předpony nemají vliv na abecední pořadí.
Tab. 1: Tvorba systematického názvu alkenů
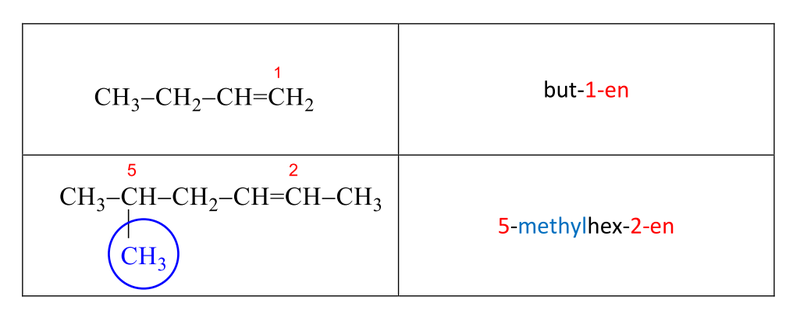
Přítomnost dvou nebo více dvojných vazeb vyjadřujeme číselnou předponou (–dien, –trien, –tetraen…) a zároveň k základu názvu přidáváme písmeno „a“.
Tab. 2: Názvosloví uhlovodíků s více dvojnými vazbami
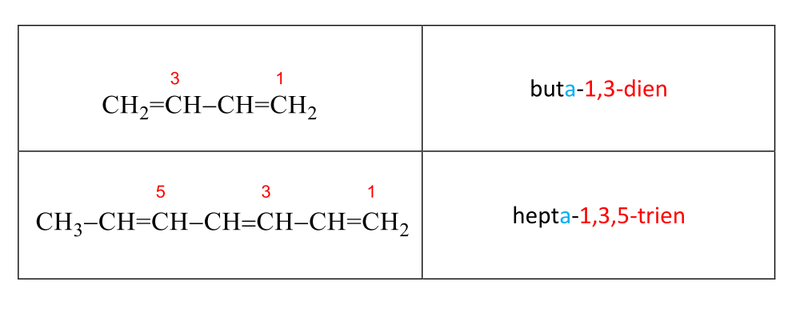
Podobně jako u alkanů získáme odtržením atomu vodíku jednovazné substituenty - alkenyly. Jejich systematické názvy tvoříme analogicky náhradou zakončení –en v názvu příslušného alkenu koncovkou –yl, přičemž uhlík, ze kterého vychází vazba, má (je-li to možné) lokant 1. U některých nižších alkenylů jsou vžité názvy triviální:
Tab. 3: Názvosloví alkenylů
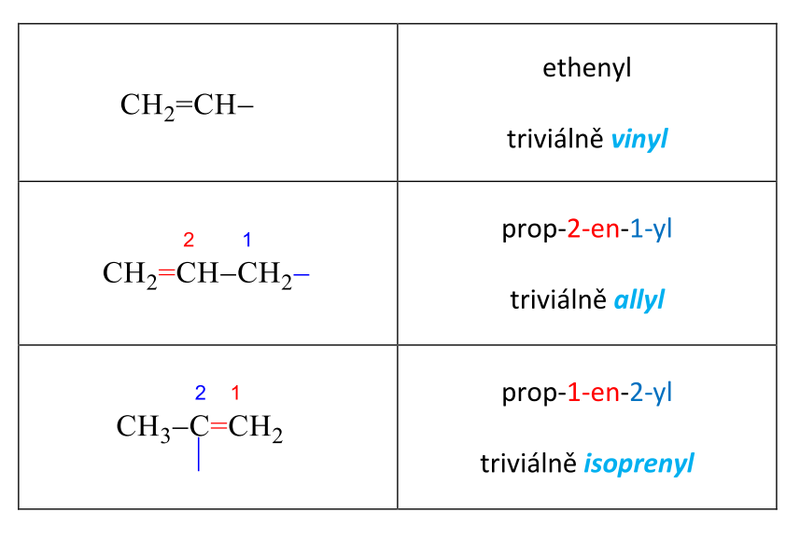
Fyzikální vlastnosti
Fyzikálními vlastnostmi se alkeny podobají alkanům.
Tab. 4: Teploty tání a varu alkenů
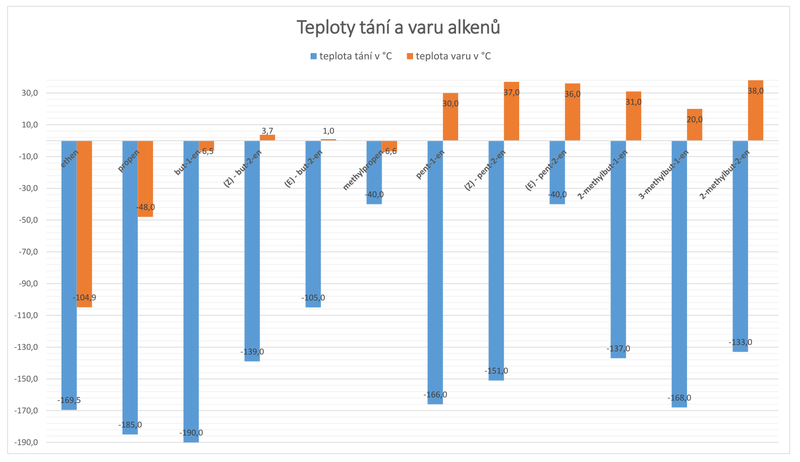
Z tabulky vyplývá, že hodnota teploty tání a varu závisí kromě počtu uhlíkových atomů v molekule a řetězové izomerii (alkeny s rozvětveným řetězcem mívají zpravidla nižší teplotu varu) také na poloze násobné vazby v řetězci (polohová izomerie) a prostorovém uspořádání skupin atomů (geometrická izomerie). E-izomery mají obvykle vyšší teplotu tání a varu než Z-izomery.
Alkeny jsou nerozpustné ve vodě, ale velmi dobře se rozpouštějí v nepolárních rozpouštědlech.
Zdroje
- FIKR, Jaroslav a Jaroslav KAHOVEC. Názvosloví organické chemie. Olomouc: Rubico, 2002, ISBN 80-7346-017-3.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 2. díl. Olomouc: Nakladatelství Olomouc, 2005, ISBN 80-7182-141-1.
- JANECZKOVÁ, Anna a Pavel KLOUDA. Organická chemie. Ostrava: Nakladatelství Pavel Klouda, 1998, ISBN 80-902155-6-4/9802.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- PACÁK, Josef. Jak porozumět organické chemii. Praha: Karolinum, 1997, ISBN 80-7184-261-3.
- SVOBODA, Jiří a kol. Organická chemie I. Praha: Vysoká škola chemicko-technologická, 2005, ISBN 80-7080-561-7.
Obrázky
- Obr. 1: Autor neznámý. chemie3d.wz.cz [online]. [cit. 25.10.2014]. Dostupný na WWW: http://chemie3d.wz.cz/images/items/trojuhelnikova.jpg
- Obr. 2: Autor neznámý. www.wikiwand.com [online]. [cit. 25.10.2014]. Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/1/11/Sp2-Orbital.svg
Pokud není uvedeno jinak, autorem obrázků je Mgr. Michal Bezděk.
Čti také
Hybridizace
Hybridizace je sjednocení energeticky různých orbitalů daného atomu, přičemž vznikají nové orbitaly, tzv. orbitaly hybridní. Hybridizace vysvětluje vznik rovnocenných kovalentních vazeb z energeticky rozdílných orbitalů a umožňuje předpovědět strukturu takto vzniklých látek.
Teorie hybridizace - video
Čti také
Hybridní stav sp2
Energetickým sjednocením jednoho orbitalu s se dvěma orbitaly p vznikají tři hybridní orbitaly sp2, které míří do vrcholů pravidelného trojúhelníku a svírají úhel 120°.

Obr. 1: Prostorové uspořádání vazeb
Obr. 2: Prostorové uspořádání hybridizovaných orbitalů
Vazby v ethenu - video
Zamysli se
S jakou jinou skupinou uhlovodíků mají alkeny stejný homologický vzorec?
Procvič si
Názvosloví alkenů - viz přílohy
Úkol
V technické praxi je velmi známá látka s názvem ethylen.
Tento název však v současné době není doporučován (ale z historických důvodů je tolerován), protože tomuto názvu odpovídají dnes dva významy.
Vyhledej v literatuře oba významy a vysvětli rozdíly mezi nimi.




