Chemické vlastnosti
Hlavním centrem reaktivity je trojná vazba. Atomy uhlíku tvořící trojnou vazbu jsou v hybridním stavu sp. Trojná vazba je tvořena jednou vazbou σ a dvěma vazbami π na sebe kolmými. Přítomností dvou vazeb π dochází ke zkrácení vazby a zvýšení její disociační energie. Protože jsou obě vazby π na sebe kolmé, vytváří kolem vazby σ souvislý válcovitý obal elektronů.
Schematické znázornění molekuly CH ≡ CH:
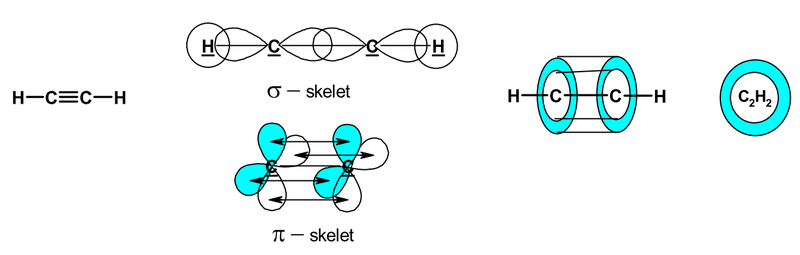
Obr. 1: Molekula ethynu
Přítomnost druhé π–vazby způsobuje, že π–elektrony jsou silněji poutány v prostoru mezi atomy uhlíku, takže elektrofilní adice probíhá v porovnání s alkeny méně snadno.
Nahuštění elektronů do prostoru mezi uhlíkové atomy způsobuje, že uhlíkové atomy zůstávají z druhé strany částečně odkryté. Proto u alkynů kromě elektrofilní adice mohou probíhat i adice nukleofilní. Uspořádání elektronů trojné vazby způsobuje, že uhlíkové atomy přitahují elektrony z vazby uhlík–vodík, který se tak může odštěpovat ve formě protonu. Říkáme, že vodík na trojné vazbě je kyselý. Účinkem silných bází (např. Na, NaNH2 ) je proto možné připravit soli alkynů - acetylidy:
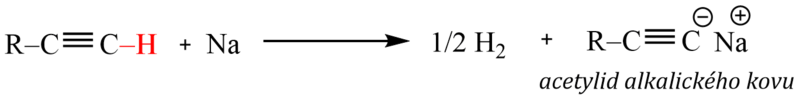
Acetylidy alkalických kovů a kovů alkalických zemin se vodou rozkládají za vzniku příslušného alkynu. Praktický význam má hydrolýza acetylidu vápníku (vžité pojmenování karbid vápníku), při které vzniká acetylen (ethyn):
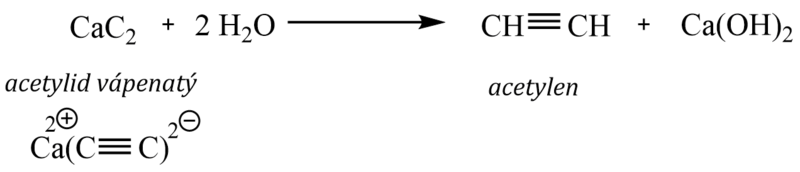
Suché acetylidy těžkých kovů (acetylid měďný, stříbrný) se explozivně rozkládají při nárazu.
Pro reaktivitu alkynů jsou charakteristické adiční reakce, při nichž se mění hybridní stav uhlíkových atomů z sp přes sp2 na sp3, a zároveň se mění délka vazby a velikost valenčního úhlu.
Charakteristické reakce alkynů jsou:
-
adiční reakce – elektrofilní, radikálové, nukleofilní,
-
polymerační reakce.
Adiční reakce alkynů
1. Adice elektrofilní (AE)
Elektrofilní adice na trojnou vazbu probíhá ve dvou stupních, i zde platí Markovnikovovo pravidlo. Jako elektrofilní činidla se uplatňují halogenvodíky, halogeny, některé minerální kyseliny, voda. Vzhledem k tomu, že elektrofilní adice probíhá u alkynů méně snadno, používají se v řadě případů jako katalyzátory soli těžkých kovů.
Adice halogenů
Na rozdíl od alkenů lze na alkyny adovat celkem dvě molekuly činidla. V prvním stupni reakce tak vznikají (E)-dihalogenalkeny, zatímco ve druhém vzniká tetrahalogenalkan. Jako příklad si uvedeme adici chloru na acetylen:
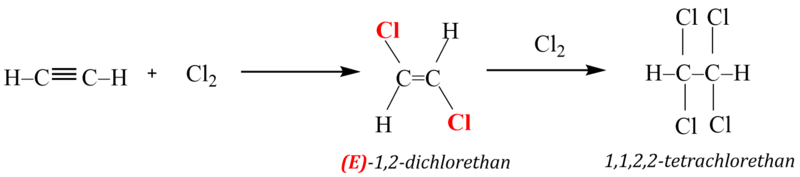
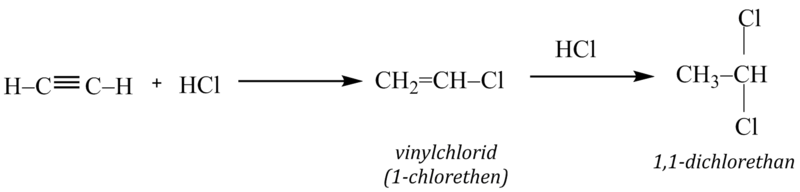
Adice halogenovodíku
Stejně jako u alkenů i tato adice nesymetrického činidla probíhá podle Markovnikovova pravidla. Opět je zde možná reakce do dvou stupňů:
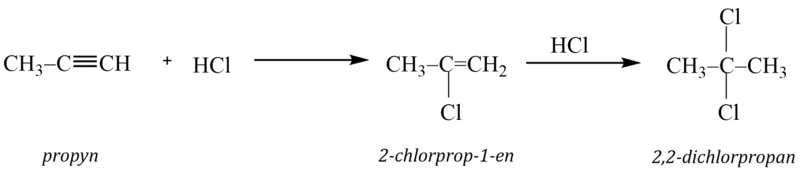
2. Adice nukleofilní (AN)
Adice vody – hydratace
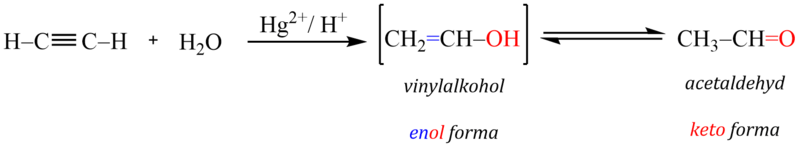
Adice vody na trojnou vazbu probíhá mechanismem nukleofilním. Technický význam má adice vody na acetylen, která probíhá v přítomnosti kyseliny sírové a síranu rtuťnatého (Kučerovova reakce). V prvním stupni reakce vzniká nestálý vinylalkohol, který se následně přesmykuje na acetaldehyd. Obdobně nestálé jsou téměř všechny sloučeniny, kde OH– skupina je vázána na uhlík, ze kterého vychází dvojná vazba.
Vinylalkohol a acetaldehyd jsou izomery, které se liší polohou dvojné vazby a jednoho atomu vodíku. Tento typ izomerie se nazývá tautomerie a jednotlivé tautomery označujeme jako enol– a ketoformu.
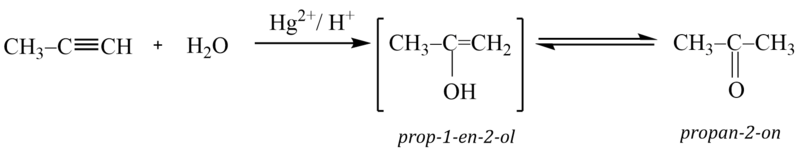
Adicí vody na další členy homologické řady alkynů vznikají ketony:
3. Adice radikálová (AR)
Adice vodíku – hydrogenace
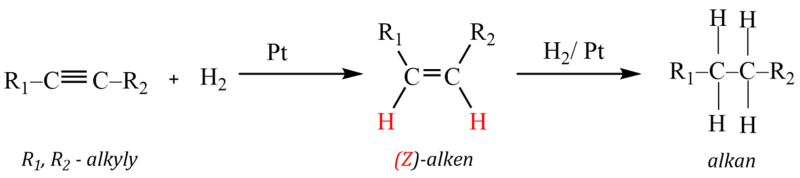
Adice vodíku na alkyny probíhá radikálovým mechanismem přes mezistadium alkenu až na alkan. Při použití obvyklých hydrogenačních katalyzátorů (Ni, Pt, Pd) vzniká přímo až alkan. Mezistadium alkenu lze zachytit pouze v případě, kdy je kovový katalyzátor vhodným způsobem deaktivován (typicky se používá malé množství chinolinu nebo octanu olovnatého). Poté je možné zastavit katalytickou hydrogenaci v prvním stupni. Takovýmto katalyzátorem je deaktivované palladium, známé též pod názvem Lindlarův katalyzátor.
Při této reakci dochází k cis adici vodíku na trojnou vazbu, která vede k alkenům s konfigurací Z (čili cis):
Stejně jako u alkenů i u alkynů je možná radikálová adice bromovodíku (Kharaschova reakce). Adice je protimarkovnikovovská.

Polymerační reakce
1. Dimerace acetylenu
Produktem reakce je vinylacetylen (but-1-en-3-yn) – významná surovina pro přípravu chloroprenu nebo butadienu (monomery pro výrobu syntetických kaučuků):
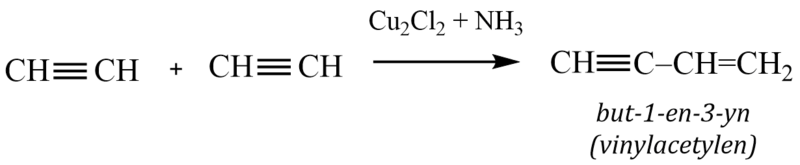

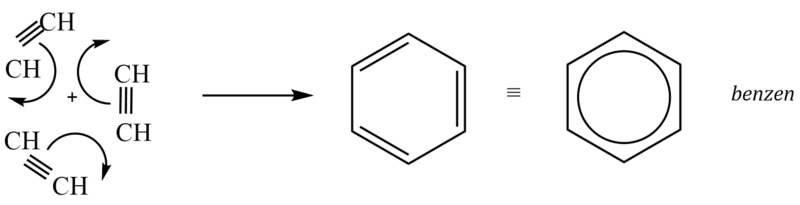
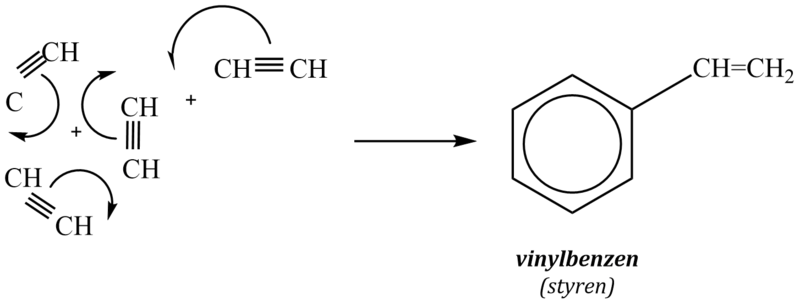
2. Trimerace a tetramerace
Trimerace a tetramerace ethynu se provádí za zvýšeného tlaku a teploty 400 až 500 °C. V prvním případě vzniká benzen, ve druhém vinylbenzen neboli styren:
Zdroje
- FIKR, Jaroslav a Jaroslav KAHOVEC. Názvosloví organické chemie. Olomouc: Rubico, 2002, ISBN 80-7346-017-3.
- HONZA, Jaroslav a Aleš MAREČEK. Chemie pro čtyřletá gymnázia 2. díl. Olomouc: Nakladatelství Olomouc, 2005, ISBN 80-7182-141-1.
- JANECZKOVÁ, Anna a Pavel KLOUDA. Organická chemie. Ostrava: Nakladatelství Pavel Klouda, 1998, ISBN 80-902155-6-4/9802.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- PACÁK, Josef. Jak porozumět organické chemii. Praha: Karolinum, 1997, ISBN 80-7184-261-3.
- SVOBODA, Jiří a kol. Organická chemie I. Praha: Vysoká škola chemicko-technologická, 2005, ISBN 80-7080-561-7.
Obrázky
- Obr. 1: STIBOR, Ivan. Dieny [online]. [cit. 31.10.2014]. Dostupný na WWW: http://old.vscht.cz/uoch/cz/studium/bakalar/organika/Velebudice/Velebudice5.pdf
- Obr. 2: Autor neznámý. www.wikiwand.com [online]. [cit. 25.10.2014]. Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/4/49/AE2h.svg
- Obr. 3: Autor neznámý. www.wikiwand.com [online]. [cit. 25.10.2014]. Dostupný na WWW: http://upload.wikimedia.org/wikipedia/commons/6/6f/VladimirMarkovnikov.jpg
- Obr. 4: Autor neznámý. media-cache-ak0.pinimg.com [online]. [cit. 25.10.2014]. Dostupný na WWW: http://media-cache-ak0.pinimg.com/736x/21/7c/e3/217ce3e771bbc94302e2bdf123db1797.jpg
Pokud není uvedeno jinak, autorem obrázků je Mgr. Michal Bezděk.
Čti také
Hybridní stav sp
Energetickým sjednocením jednoho orbitalu s s jedním orbitalem p vznikají dva hybridní orbitaly sp, které svírají úhel 180°, a molekula má tvar přímky.
Obr. 2: Prostorové uspořádání hybridizovaných orbitalů
Teorie hybridizace - video
Hybridní stav - video
Vazby v ethynu - video
Adice
Adice je reakce, při které dochází k zániku vazby π a k navázání atomu či skupiny atomů sigma vazbou. Z jedné dvojné vazby tedy vznikají dvě jednoduché.
Elektrofilní činidlo (elektrofil)
Elektrofil je částice s nedostatkem elektronů, která na substrátu napadá místo s největší elektronovou hustotou. Má povahu kationtu, zpravidla se zapisuje jako E nebo E+.
Nukleofilní činidlo (nukleofil)
Nukleofil je částice s nadbytkem elektronů, která na substrátu napadá místo s nejmenší elektronovou hustotou. Má povahu aniontu nebo molekuly s volným elektronovým párem (páry).
Geometrické izomery
Jedná se o izomery lišící se konfigurací substituentů na dvojné vazbě nebo na cyklu. Nachází-li se substituenty na stejné straně dvojné vazby, označujeme tento izomer jako Z (starším cis), jsou-li na opačných stranách, jako izomer E (starším trans). Jako pomůcka pro zapamatování se vžilo spojení s německými slovy „entgegen“ (naproti) a „zusammen“ (spolu, dohromady).
geometrická izomerie
Čti také
Tautomerie
Tautomerie je druh izomerie organických sloučenin, kdy jednotlivé izomery, tzv. tautomery, se liší polohou dvojné vazby a polohou jednoho z vodíkových atomů.
Izomer s vazbou C=C a hydroxylovou skupinou se jmenuje enolforma (název vznikl spojením systematických přípon –en a –ol).
Izomer s vazbou C=O se nazývá keto(oxo)forma. Enolforma je ve většině případů nestabilní a okamžitě se přesmykuje na ketoformu.
K jakému druhu izomerie řadíme tautomerii?
Ketony
Ketony jsou deriváty uhlovodíků obsahující karbonylovou funkční skupinu, na kterou jsou navázány dva uhlovodíkové zbytky (stejné nebo různé).
Procvič si
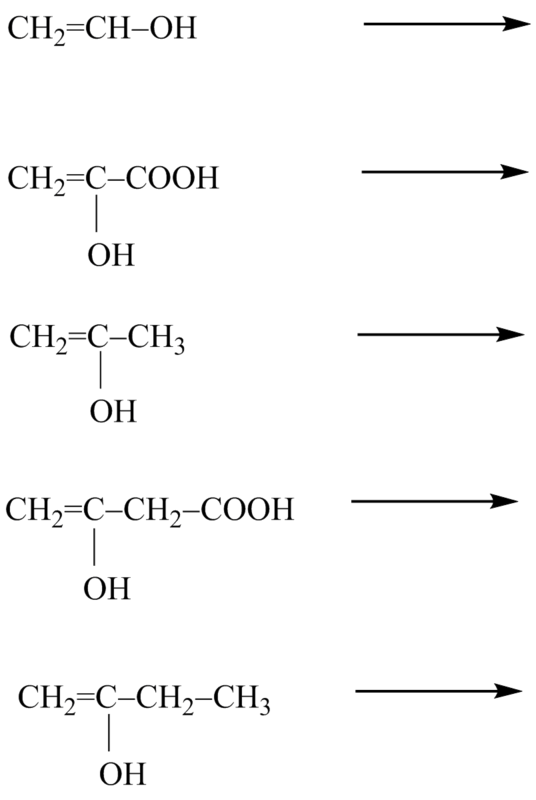
K zadaným enol tautomerům vytvoř jejich keto formy:
Čti také
Dimerace
Dimerace je reakce (spojení) dvou molekul monomeru.
Trimerace
Trimerace je reakce (spojení) tří molekul monomeru.
Tetramerace
Tetramerace je reakce (spojení) čtyř molekul monomeru.
Chloropren
Chloropren je surovina k výrobě chloroprenového kaučuku, známého pod názvem Neopren, který slouží jako materiál k výrobě kombinéz pro vodní sporty.
Benzen
Bezbarvá kapalina s charakteristickým zápachem, známá svými karcinogenními účinky. Benzen se používá jako surovina pro výrobu celé řady chemických látek.
Styren
Bezbarvá olejovitá kapalina se sladkým zápachem. Je špatně rozpustný ve vodě. Snadno podléhá polymeraci, při níž vzniká polystyren, nebo kopolymeračním reakcím za vzniku různých druhů kaučuků (např. butadien-styrenový kaučuk).






