Monosacharidy
Obsahují ve svých molekulách 3 až 7 atomů uhlíku. Jsou to bílé krystalické látky, sladké chuti, rozpustné ve vodě a etanolu. Zahříváním tají, při vyšší teplotě hnědnou (karamelizují). Monosacharidy podléhají přeměnám, které způsobují různé mikroorganismy, například kvasinky (lihové kvašení).
Jsou základní stavební jednotkou pro oligosacharidy a polysacharidy.
Z chemického hlediska jsou to polyhydroxyaldehydy a polyhydroxyketony. Ve svých molekulách obsahují hydroxy skupiny OH a funkční aldehydové skupiny a funkční ketonové skupiny.
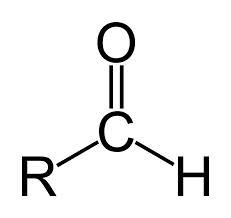
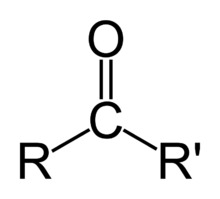
Obr.1: Struktura aldehydové a ketonové skupiny
Podle toho, jakou funkční skupinu jednotlivé monosacharidy obsahují, je dělíme na:
- Aldózy- obsahují aldehydovou funkční skupinu
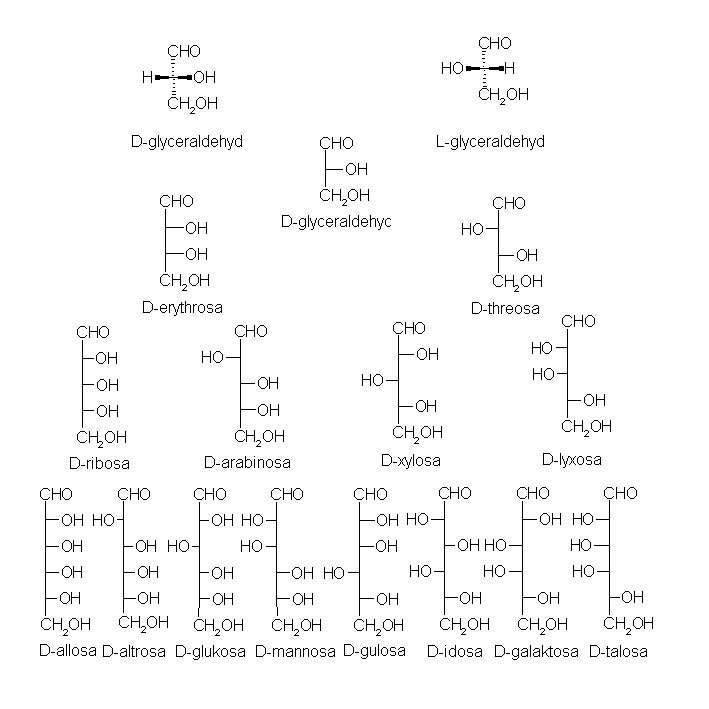
Obr.2: Genetická řada aldóz
2.Ketózy- obsahují ketonovou funkční skupinu
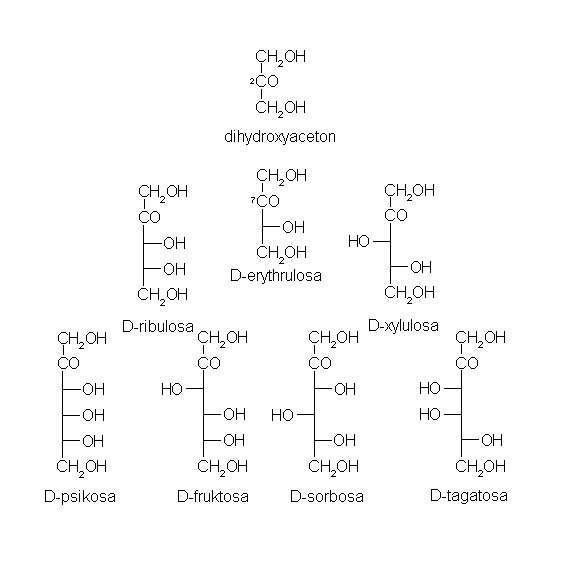
Obr. 3: Genetická řada ketóz
Základ obou tabulek představuje tříuhlíkatý cukr, od kterého následně odvozujeme další řadu přidáním uhlíku s hydroxy skupinou a vodíkem pod funkční skupinu (aldehydovou nebo ketonovou).
Podle počtu uhlíků dělíme monosacharidy na:
-
Triózy- mají ve své molekule 3 uhlíky
-
Tetrózy- mají ve své molekule 4 uhlíky
-
Pentózy- mají ve své molekule 5 uhlíků
-
Hexózy- mají ve své molekule 6 uhlíků
-
Heptózy- mají ve své molekule 7 uhlíků
Př.: Glukózu řadíme do aldóz a hexóz, je to tedy aldohexóza.
Optická aktivita cukrů
Opticky aktivní látka je schopná stáčet rovinu polarizovaného světla o určitý úhel.
Takovéto látky obsahují nejméně jeden asymetrický-chirální uhlík. Chirální uhlík obsahuje na každé své vazbě navázaný jiný substituent.
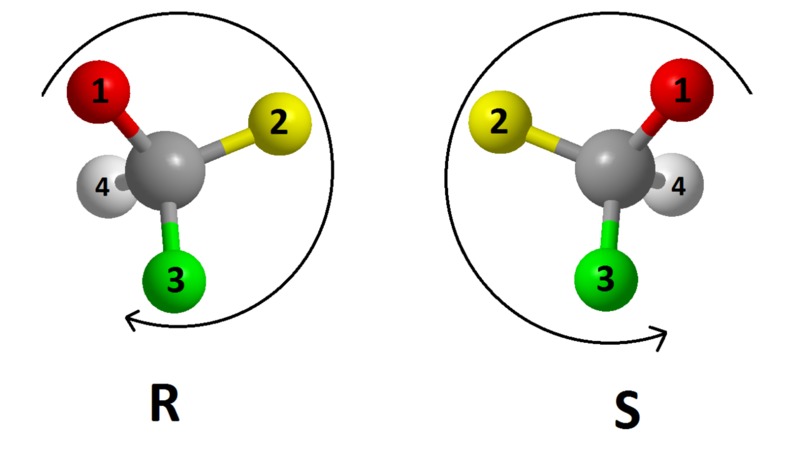
Obr. 4: Znázornění různého uspořádání substituentů na centru chirality (atomu uhlíku).
Nejjednodušší cukr aldotrióza je glyceraldehyd a má 1 asymetrický uhlík.
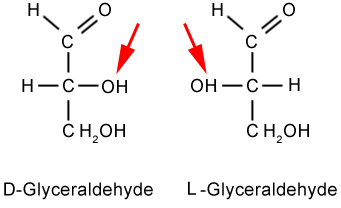
Obr. 5: D-glyceraldehyd a L-glyceraldehyd
Podle polohy hydroxy skupiny na asymetrickém uhlíku rozlišujeme 2 optické izomery. Tyto izomery označujeme jako enantiomery.
D- enantiomer má na posledním asymetrickém uhlíku OH skupinu vpravo,
L- enantiomer má OH skupinu na posledním asymetrickém uhlíku vlevo.
Jednotlivé enantiomery tedy vypadají jako obraz v zrcadle.
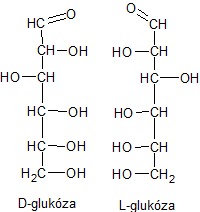
Obr. 6: D a L-glukóza
Racemická směs- je směs izomerů D a L v poměru 1:1, tato směs nestáčí rovinu polarizovaného světla o žádný úhel.
Mimo enantiomerů tvoří monosacharidy ještě další typy izomerů:
Epimery-jsou optické isomery, které se liší polohou OH skupiny na asymetrickém uhlíku ležící nejblíže funkční skupině, například glukóza a manóza.
Anomery-monosacharidy snadno vytvářejí pětičlenné nebo šestičlenné cyklické kruhy. Při cyklizaci se na 1. uhlíku vytváří další asymetrické centrum. Rozlišujeme 2 typy těchto izomerů:
Alfa anomery mají -OH skupiny vpravo (pod rovinou).
Beta anomery mají -OH skupinu vlevo (nad rovinou).
K cyklizaci dochází díky poloacetalové nebo poloketalové reakci. Jedná se o reakci funkční skupiny s hydroxyskupinou na posledním asymetrické uhlíku.
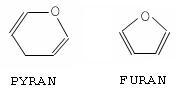
Pětičlenné cykly odvozujeme od furanu a šestičlenné od pyranu.
K přepisu dochází následujícím způsobem:
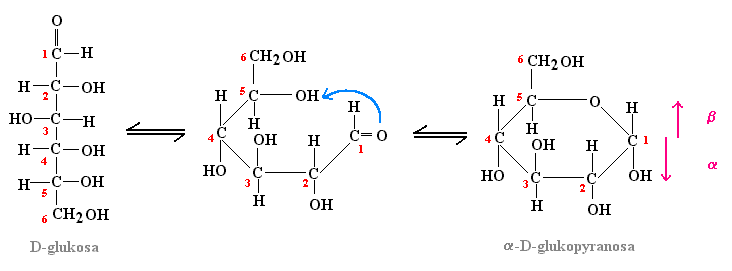
Obr. 7: Přepis glukózy do Haworthova vzorce
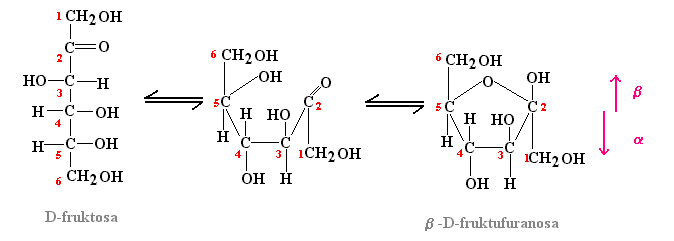
Obr. 8: Přepis fruktózy do Haworthova vzorce
Chemické vlastnosti monosacharidů:
- Monosacharidy obsahují na C1 aldehydovou neboli poloacetalovou skupinu, díky níž mají redukční vlastnosti. Tedy jsou schopné se oxidovat (aldehydová skupina se oxiduje na karboxylovou kyselinu). K oxidaci může docházet rovněž na C6, kdy se alkoholová skupina oxiduje na karboxylovou kyselinu.Postupně tak vznikají kyseliny aldonové, uronové až aldarové.
2.Reakce s kyselinami: monosacharidy s organickými i anorganickými kyselinami tvoří estery.
3.Reakce s alkoholy: poloacetalová hydroxylová skupina reaguje s alkoholy za vzniku etherů.
4.Kvašení cukrů: kvašení monosacharidů se účastní kvasinky rodu Saccharomyces cerevisiae. Vzniká při něm oxid uhličitý a etanol.
Některé významné monosacharidy:
D-glyceraldehyd a dihydroxyaceton jsou nejjednodušší monosacharidy, jsou součástí metabolismu glukózy, tzv. glykolýzy.
D-ribóza a D-deoxyribóza jsou součástí nukleotidů v nukleových kyselinách
D-xylóza se využívá v klinické biochemii k zátěžovému testu na ověření kvality resorpce v tenkém střevě.
D-glukóza (dextróza, hroznový cukr) je nejběžnější monosacharid. Je to bílá sladká látka, dobře rozpustná ve vodě.Vyskytuje se v ovoci, medu a rostlinných šťávách.Představuje ideální živinu pro organismus, protože ji dokáží metabolizovat všechny tkáně včetně mozkové. Díky tomu se užívá při umělé výživě v infuzích.Fyziologická koncentrace glukózy v krvi je 3,5-5,6 mmol/l.
D-galaktóza tvoří základ polysacharidu agaru, který se využívá jako živná půda v mikrobiologii.
D- fruktóza (levulóza, ovocný cukr) je obsažena v cukerných šťávách a medu a je nejsladším cukrem.V těle vzniká hlavně štěpením sacharózy.
Zdroje
- BENEŠOVÁ, Marika a Hana SATRAPOVÁ. Odmaturuj! z chemie. Vyd. 1. Brno: Didaktis, 2002. 208 s.ISBN 80-86285-56-1.
- DURČÁKOVÁ, Zdenka et al. Chemické pokusy pro žáky základních škol. Vyd. 1. Olomouc: Univerzita Palackého, 2001. 177 s, ISBN 80-86238-17-2
- HOLEČEK, Václav, Luboš STÁRKA a Emil BIELIK. Biochemie. 1. vydání. Praha: Avicenum,zdravotnické nakladatelství, 1983.
- KOTLÍK, Bohumír a Květoslava RŮŽIČKOVÁ. Chemie v kostce II.. Havlíčkův Brod: Fragment, 1997, ISBN 80-7200-342-9.
- Lékařská chemie a biochemie: učebnice pro lékařské fakulty. 1. vyd. Praha: Avicenum, 1991. 661 s.ISBN 80-201-0114-4.
Obrázky
- Obr. 1: Autor neznámý. http://www.referaty22.8u.cz [cit. 26.10. 2014] Dostupné na www: http://www.referaty22.8u.cz/chemie/ketony/
- Obr. 2: Autor neznámý.http://naturstoff.sweb.cz [cit. 4. 4. 2014] Dostupné na www: http://naturstoff.sweb.cz/chemdir/sacharidy/aldosy-vz.html
- Obr. 3: Autor neznámý.http://naturstoff.sweb.cz [cit. 4. 4. 2014] Dostupné na www: http://naturstoff.sweb.cz/chemdir/sacharidy/ketosy-vz.html
- Obr. 4: : Autor neznámý.http://cs.wikipedia.org [cit. 20. 4. 2014] Dostupné na www: http://cs.wikipedia.org/wiki/Chiralita
- Obr. 5: Autor neznámý. http://www.ncl.ac.uk [cit. 15.1. 2014] Dostupné na www:http://www.ncl.ac.uk/dental/oralbiol/oralenv/tutorials/polysaccharides/basics.htm
- Obr. 6: Autor neznámý:http://www.mojechemie.cz [cit. 5. 11. 2013] Dostupné na www: http://www.mojechemie.cz/images/D_a_l_glukoza.png
- Obr. 7: Autor neznámý. http://projektalfa.ic.cz [cit. 9. 9. 2014] Dostupné na www: http://projektalfa.ic.cz/monosacharidy.htm
- Obr. 8: Autor neznámý. http://projektalfa.ic.cz [cit. 9. 9. 2014] Dostupné na www: http://projektalfa.ic.cz/monosacharidy.htm
- Obr. 9: Autor neznámý. http://www.pivniklenoty.cz [cit. 25.10.2014] Dostupné na www: http://www.pivniklenoty.cz/vse-o-pivu/zajimavosti-o-pivu/kvasnice-kvaseni-a-jeho-druhy/
- Obr. 10: Autor neznámý.http://www.hospodynkam.cz [cit. 6.3. 2014] Dostupné na www: http://www.hospodynkam.cz/Agar-50g-d1386.htm
- Obr. 11: Autor neznámý. http://www.carnicominstitute.org [cit. 3. 11. 2013] Dostupné na www:http://www.carnicominstitute.org/articles/bio11.htm
- Obr. 12: Archiv autora
- Obr. 13:Autor neznámý. http://prozeny.blesk.cz [cit. 20.9. 2014] Dostupné na www:http://prozeny.blesk.cz/clanek/pro-zeny-diety/133638/ovocne-diety-nezhubnete-zato-vam-znici-zuby.html
- Obr. 14: Archiv autora
- Obr. 15: Autor neznámý. http://polar-peza.euweb.cz [cit. 19. 11. 2013] Dostupné na www: http://polar-peza.euweb.cz/vyuziti_polarizace.html
- Obr. 16: Autor neznámý. www.wikipedia.org [cit. 19. 11. 2013] Dostupné na www: http://en.wikipedia.org/wiki/Tollens'_reagent
Kontrolní otázka
Chemická struktura monosacharidů
Zařaďte do systému monosacharidů podle funkční skupiny a podle počtu uhlíků:
a) D- xylózu
b) D- manózu
c) D-sorbózu
d) D- fruktózu
Zajímavost
Glykémie, glykosurie
Hladinu glukózy v krvi označujeme glykémie. Při snížení hladiny glukózy v krvi pod 3,5mmol/l dochází k hypoglykémii, při zvýšení hladiny nad 5,6 mmol/l dochází k hyperglykémii. K těmto poruchám dochází u onemocnění diabetes mellitus. Pokud se zvýší hladina glukózy v krvi nad 11 mmol/l, dochází k vylučování glukózy močí – glykosurie.
V důsledku některých patologických stavů může někdy docházek k vylučování monosacharidů do moči, např. vylučování pentóz do moči označovaný jako pentosurie, nebo vylučování glukózy do moči glykosurie, galaktózy galaktosurie.
Zajímavost
Umělá sladidla
Redukcí glukózy vzniká glucitol neboli sorbitol, který se využívá jako umělé sladidlo pro diabetiky.
Laboratorní cvičení
Důkazové reakce sacharidů I
Redukční vlastnosti monosacharidů lze dokázat Fehlingovou reakcí. Principem této reakce je redukce měďnatých kationtů v roztoku na oxid měďný.
Obr. 12: Fehlingova činidla
Návod k úloze naleznete v hlavním textu v přílohách.
Laboratorní cvičení
Důkazové reakce sacharidů II
Další možnosti důkazu monosachariů je Tollensova reakce, kdy dochází k redukci stříbrných kationtů z roztoku na stříbro. Návod naleznete v hlavním textu v přílohách.
Laboratorní cvičení
Důkaz monosacharidů v potravinách
V hlavním textu v přílohách najdete návod na důkaz monosacharidů v potravinách.

Obr. 13: Ovoce
Doplňující učivo
Polarizované záření, polarimetr
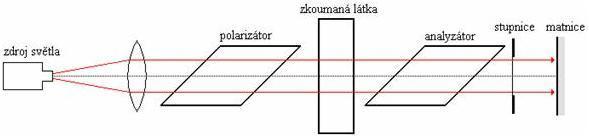
Normální světlo se skládá z elektromagnetických vln, které kmitají ve všech směrech, kolmo na zdroj svého šíření. Jestliže do cesty tomuto svazku paprsků vložíme polarizační zařízení např. Nikolův hranol, získáme záření nezměněné vlnové délky, ale kmitající v jedné rovině.
Přístroj, kterým měříme úhel otočení polarizovaného světla nazýváme polarimetr.
Doplňující učivo
Redukční vlastnosti monosacharidů
Redukční vlastnosti monosacharidů lze dokázat Fehlingovou reakcí.Principem této reakce je redukce měďnatých kationtů v roztoku na oxid měďný.
Další možnosti je důkaz Tollensovou reakcí, kdy dochází k redukci stříbrných kationtů z roztoku na stříbro.