Thioly a sulfidy
Tab. 1: Porovnání struktury kyslíkatých a sirných derivátů
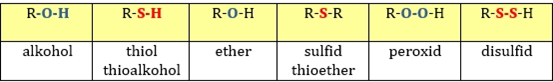
Thioly (thioalkoholy, thiofenoly, merkaptany) R-SH
Charakteristika
Obsahují funkční sulfanylovou (thiolovou) skupinu –SH; lze je odvodit nahrazením atomu kyslíku v hydroxylové skupině -OH alkoholu nebo fenolu atomem síry nebo odvozením od molekuly sulfanu.
Obecný vzorec: R - SH
Názvosloví
Název základního uhlovodíku (hydridu) + koncovka –thiol, dithiol.
Jestliže není –SH hlavní skupinou, pak se její přítomnost vyjadřuje předponou sulfanyl – (dříve merkapto -)
Tab. 2: Příklady názvů thiolů
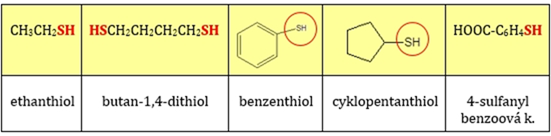
Příprava
Provádí se zahřívání alkoholických roztoků příslušného alkylhalogenidu a hydrogensulfidu. Hydrogensulfid se připravuje probubláváním sulfanu přes alkoholický roztok hydroxidu. Hydrogensulfid musí být použit ve stechiometrickém přebytku, jinak dochází k následné nežádoucí reakci s halogenalkanem na symetrický sulfid.
Příprava alkanthiolu: RBr +KHS → RSH + KBr (R-SH + R-Br → R-S-R)
V aromatické řadě se používají spíše jiné postupy, např. redukce chloridů příslušných aromatických kyselin.V průmyslu se thioly nejčastěji vyrábějí reakcí odpovídajícího alkoholu se sulfanem H2S v kyselém prostředí:
CH3OH + H2S → CH3SH + H2O
Vlastnosti
Jedná se o sirné obdoby alkoholů a fenolů. Jsou kyselejší, mají ale obdobné reakce. Netvoří vodíkové můstky, proto mají nižší teploty tání a varu než odpovídající alkoholy a fenoly. Jedná se o plyn (methanthiol) a kapaliny charakteristického, velmi nepříjemného pronikavého zápachu (3-methylbutan-1-thiol je obsažen v sekretu skunkovitých šelem). Způsobují i charakteristický pach mléka, mléčných výrobků a dále i česneku (allylthiol) a cibule (propan-1-thiol). Ve vodě jsou nerozpustné, rozpustné jsou v ethanolu a diethyléteru.
Tab. 3: Porovnání teploty tání a varu alkan - thiol - alkohol
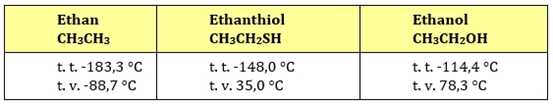
Vznik thiolátů
Mezi sírou a vodíkem je slabá vazba, která způsobuje, že thioly jsou kyselejší než alkoholy. Reakcí thiolu s vodným roztokem bazického hydroxidu vznikají thioláty:
CH3CH2-SH + NaOH → CH3CH2-SNa + H2O
Oxidace thiolů
Thioly se snadno oxidují. Mírnou oxidací (při použití slabých oxidovadel; brom, jod) vznikají disulfidy:
2 C2H5SH → C2H5 - S-S - C2H5 diethyldisulfid
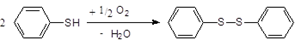 difenyldisulfid
difenyldisulfid
Silnou oxidací (peroxid vodíku) vznikají sulfonové kyseliny:
C2H5SH → C2H5SO3H kyselina ethansulfonová
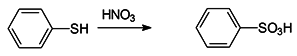 kyselina benzensulfonová
kyselina benzensulfonová
Zástupci
CH3SH methanthiol je odporně zapáchající plyn, vzniká rozkladem bílkovin ve střevech.
C2H5SH ethanthiol je zapáchající kapalina, dříve odorizace svítiplynu a zemního plynu, aby byly čichově zjistitelné.
C4H9SH butanthiol + CH3CH(CH3)CH2CH2SH 3-methylbutan-1-thiol jsou součástí sekretu tchoře a skunka.
C6H5SH benzenthiol zapáchající toxická kapalina, výroba sirných barviv.
V neživé přírodě se thioly vyskytují v ropě, uhlí a kondenzátu zemního plynu. Zemní plyn těžený v Kataru a Íránu obsahuje až 3000 ppm thiolů. V energetice způsobují thioly problémy svou přítomností ve skládkovém plynu a bioplynu. Thioly způsobují u nesprávně skladovaných vín charakteristický zápach, který má za následek jejich znehodnocení.

Obr. 1: Skunk pruhovaný

Obr. 2: Tchoř tmavý
Sulfidy (thioethery) R-S-R´
Charakteristika
Obsahují funkční sulfidickou skupinu –S–; lze je odvodit nahrazením atomu kyslíku v etherové skupině –O– atomem síry; případně odvozením od molekuly sulfanu nahrazením atomů vodíku uhlovodíkovými zbytky.
Obecný vzorec: R - S - R´
Názvosloví
Název alkylů (řazeno podle abecedy) + koncovka – sulfid
Příklady názvů sulfidů
Vlastnosti
Mají méně nepříjemný zápach než thioly, teploty varu jsou obdobné jako u thiolů se stejnou molekulovou hmotností.
Příprava sulfidů
Reakce alkylhalogenidu a sulfidu:
2C2H5Br +K2S → C2H5 -S-C2 H5 + 2KBr

Obr. 3: Česnek a cibule jako zdroj diethylsulfidu

Obr. 4: Molekula Yperitu
Zástupci
CH2=CH-CH2-S-CH2-CH=CH2 diallylsulfid (DAS)
CH2=CH-CH2-S-S- CH2-CH=CH2 diallyldisulfid (DADS) oba jsou obsaženy v silici cibule a česneku, mají protinádorové účinky.
(CH2-CH2-Cl)2S bis(2-chlorethyl)sulfid yperit (hořčičný plyn) název podle belgického města Ypres; bojový chemický zpuchýřující plyn, způsobuje poranění kůže a dýchacích cest.
Zdroje
- VÍCHA, Robert. WWW.CHEMIE.UTB.CZ. [online]. [cit. 2014-18-05]. Dostupné z: http://www.chemie.utb.cz/rvicha/SOC/supportfiles/DOCS/sira.doc
- HOFFMEIER, Klaus. WIKIPEDIA.ORG. Glucosinolates [online]. [cit. 5.11. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Brukvovit%C3%A9#mediaviewer/File:Glucosinolates.png
- WIKIPEDIA.ORG. Thioly [online]. [cit. 5.11. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Thiol
Obrázky
- Obr. 1: Skunk pruhovaný [online]. [cit. 2014-10-22]. Dostupné z: http://commons.wikimedia.org/wiki/File:Striped_skunk.jpg
- Obr. 2: MALENE, Thyssen. Tchoř tmavý [online]. [cit. 5.11. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Tcho%C5%99_tmav%C3%BD#mediaviewer/File:Ilder.jpg
- Obr. 3: Archiv autora
- Obr. 4: MILLS, Ben.WIKIPEDIA.ORG. Molekula yperitu [online]. [cit. 5.11. 2014]. Dostupné z: http://upload.w ikimedia.org/wikipedia/commons/4/4c/Sulfur-mustard-3D-vdW.png
- Obr. 5: VINCENTZ, Frank. WIKIPEDIA.ORG. Armoracia rusticana - Kořen křenu [online]. [cit. 5.11. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Křen#mediaviewer/File:Armoracia_rusticana_03_ies.jpg
- Obr. 6: WIKIPEDIA.ORG. Oběť války v Iráku 1980 zasažená Yperitem [online]. 31.10.2004 [cit. 4.11. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Yperit
- Obr. 7: Youtube.com.Plynový útok [online].[cit. 4.11. 2014]. Dostupné z: https://www.youtube.com/watch?feature=player_embedded&v=22w1UVGv71M
Doplňující učivo
Fytoalexiny
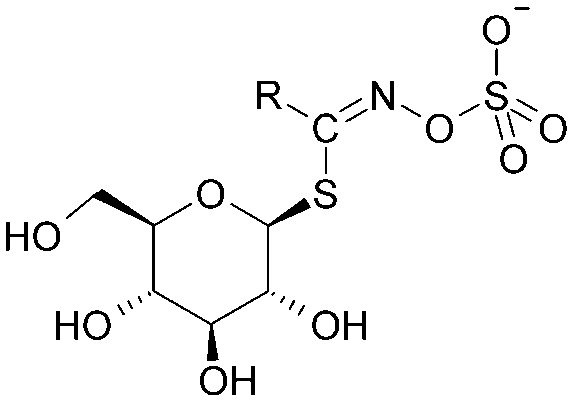
"Jsou rostlinná antibiotika, rostlinu chrání před bakteriemi a plísněmi. Rostlina je začne produkovat při napadení houbou, jiným organismem, toxickou látkou nebo zářením. Hromadí se především v listech, plodech a kořenech. Často jsou příčinou výrazné chuti rostlin. Sirné fytoalexiny se vyskytují ve větší míře v brukvovitých rostlinách (brassinin - řepka, sinigrin a glukonasturtiin – hořčice, sinigrin – křen, aj.)" (1)
Obecný vzorec glukosinolátu (2)

Obr. 5: Kořen křenu
Čti také
YPERIT
Jako chemické zbraně se během 1. světové války používaly chlor a fosgen od roku 1915. V roce 1917 se bitvě u Ypres poprvé použil nový plyn s hořčičným zápachem, který získal název podle místa použití yperit. Yperit byl objeven Frederikem Guthrie ale již v roce 1860, v roce 1916 vynalezli němečtí chemici Wilhelm Lommell a Wilhelm Steinkopf pouze způsob, jak produkovat plyn masově pro bojové účely. Tato látka patří do skupiny zpuchýřujících bojových látek, projevuje se leptáním sliznic. Proniká do organismu oděvem a všemi cestami vstupu – kůží, dýchacími orgány, očními spojivkami i zažívacím ústrojím. Otravy se projevují obvykle za 4-6 hodin po zasažení. Proti novému plynu nepomáhaly plynové masky, leptal kůži a ve velkém vyřazoval nepřátelské vojáky z boje. Má na svědomí kolem 400 000 obětí během 1. světové války. Má poměrně velkou trvanlivost a území zůstává zamořeno řadu dnů. Použit byl i později, např. Irák proti Kurdům v roce 1988.
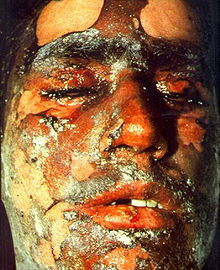
Obr. 6: Oběť války v Iráku zasažená hořčičným plynem
Po první světové válce došlo k výzkumu působení na nádorové buňky. Z yperitu vycházejí první cytostatika.
Úkol
Navrhni přípravu:
-
ethanthiolu
-
dipropylsulfidu
Znázorni rovnicí:
-
mírnou oxidaci benzenthiolu
-
silnou oxidaci benzenthiolu
Zapamatuj si
Odorizace
Je čichové označení topných nebo jedovatých plynů, slouží k signalizaci úniku těchto plynů. Používá se v plynárenském a chemickém průmyslu. Obvykle se odorizuje thioly nebo sulfidy. Odorizace způsobuje, že plyn získá typický zápach, podle kterého se pozná únik a je ho možno ihned odstranit.




