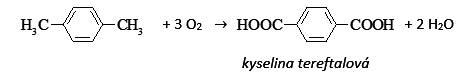Příprava a výroba kyselin
Mezi průmyslovými výrobami i v laboratorní přípravě převládají metody oxidační, výchozími surovinami jsou primární alkoholy, aldehydy, aromatické uhlovodíky s bočními řetězci i další nasycené i nenasycené uhlovodíky.
Oxidace probíhají v řadě: R-CH3 → R-CH2-OH → R-CH=O → R-COOH.
Kromě oxidací se využívají i hydrolytické a biochemické metody.
Oxidace alkanů a cykloalkanů
Probíhá za přítomnosti katalyzátorů, vzniká vždy pestrá směs kyslíkatých produktů, proto je význam metody poměrně malý. Významná je výroba kyseliny adipové, v prvním stupni dochází k hydrogenaci benzenu na cyklohexan a v 2. stupni probíhá oxidace buď účinkem 60% kyseliny dusičné, nebo moderněji použitím vzdušného kyslíku za přítomnosti katalyzátoru. Nejpoužívanější je ale v současné době obdobná oxidace směsi cyklohexanolu a cyklohexanonu. Základní surovinou je v tomto případě fenol:
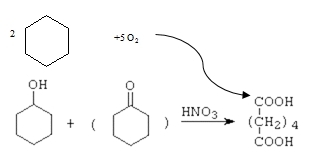
Výroba kyseliny adipové
V případě kyseliny octové lze využít přímé oxidace směsi nižších alkanů, především s obsahem butanu:
2 CH3CH2CH2CH3 + 5 O2 → 4 CH3COOH + 2 H2O.
Oxidace arenů
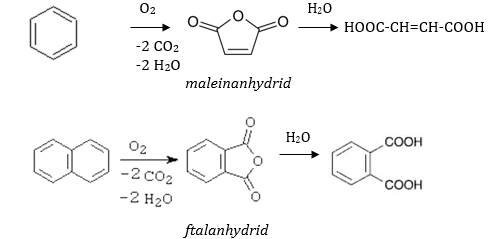
Probíhá katalyticky při vyšší teplotě, dochází k destrukci aromatického jádra. Významná je oxidace benzenu za vzniku maleinanhydridu nebo naftalenu za vzniku ftalanhydridu, následnou hydrolýzou anhydridů vznikají příslušné kyseliny. Velký význam má i oxidace p- xylenu na kyselinu tereftalovou (výrobní postup ve skutečnosti probíhá ve 4 stupních).
Oxidace alkenů
Probíhá snadno, jako oxidační činidlo lze použít vodný roztok manganistanu, průmyslově kyslík za přítomnosti katalyzátoru. Průmyslově má velký význam např. výroba kyseliny akrylové katalytickou oxidací (vzdušným kyslíkem) propenu:
CH2 = CH - CH3 + 3/2 O2 → CH2 = CH - COOH + H2O
Oxidace aromátů s vedlejším řetězcem
Jedná se o průmyslově významné oxidace. Tímto způsobem se vyrábí například kyselina benzoová, kyselina ftalová a kyselina tereftalová.
C6H5 -CH3 + 3/2 O2 → C6H5 -COOH + H2O t = 120°C, kat. Co2+
Oxidace aldehydů a ketonů
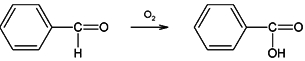
Lze použít obecně pro kterékoliv kyseliny. Při použití ketonů jako výchozích látek dochází k jejich oxidačnímu štěpení. Průmyslově nejvýznamnější je výroba kyseliny octové z acetaldehydu za přítomnosti katalyzátoru (octany Co, Mn); obdobně lze připravit například kyselinu benzoovou z benzaldehydu:
CH3CHO + 1/2 O2 → CH3COOH t = 50 - 70°C, kat.Co2+
Oxidace alkoholů
Méně významné, používají se vyšší teploty, silnější oxidační činidla a vzniká bohatší směs produktů.
Hydrolýza funkčních derivátů kyselin
Lze použít u všech derivátů, nejsnadněji probíhá u halogenidů, je vhodná jako laboratorní příprava:
RCOCl + H2O ⇆ RCOOH + HCl
Největší význam má však hydrolýza esterů. Vyšší mastné kyseliny se získávají hydrolýzou tuků; alkalickou hydrolýzou (zmýdelňováním) vznikají soli karboxylových kyselin (ve skutečnosti směs), tedy mýdla:
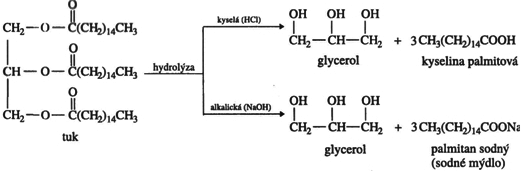
Hydrolýza glyceridů (tuků) - kyselá hydrolýza a zásaditá (zmýdelňování)
Další postupy
Kyselina mravenčí se vyrábí několika postupy, vždy se ale jako výchozí látka používá oxid uhelnatý. Jedná se o syntézy oxidu uhelnatého s hydroxidem sodným, amoniakem nebo nejnověji s methanolem:
CO + NaOH → HCOONa následuje vytěsnění kyselinou sírovou:
2 HCOONa + H2SO4 → 2 HCOOH + Na2SO4
Při výrobě kyseliny octové se moderně používá karbonylace methanolu, reakce je třístupňová:
CH3OH + CO → CH3COOH (souhrnná reakce)
Děj probíhá za přítomnosti jodovodíku a komplexních katalyzátorů s obsahen palladia nebo rhodia a iridia. Meziproduktem je jodmethan:
CH3OH + HI → CH3I + H2O
CH3I + CO → CH3COI
CH3COI + H2O → CH3COOH + HI.
Biochemické výroby
Průmyslově se využívají pro výrobu kyseliny octové, citronové a mléčné (viz prezentace).
Kyselina octová se vyrábí z ethanolu oxidativní fermentací pomocí octových tyčinkových bakterií (Acetobacter).
Kyselina mléčná fermentací melasové sacharozy mléčnými tyčinkovými bakteriemi (Lactobacillus delbrückii).
Kyselina citronová aerobní fermentací melasové sacharozy pomocí plísně (Aspergillus niger).
Zdroje
- CANOV, Michael. [online]. [cit. 2014-4-19]. Dostupné z: http://canov.jergym.cz/
- WIKIPEDIA.ORG. [online]. [cit. 2014-4-19]. Dostupné z: http://cs.wikipedia.org/wiki/Karboxylov%C3%A9_kyseliny
Obrázky
- Obr. 1: COMMONS.WIKIMEDIA.ORG. [online]. [cit. 29.10.2014]. Dostupné z: http://commons.wikimedia.org/wiki/File:Essig-1.jpg
- Obr. 2: Archiv autora
Laboratorní cvičení
Laboratorní cvičení z OCH
- příprava kyseliny octové
- vlastnosti kyseliny octové
- příprava kyseliny benzoové

Obr. 2: Syntéza kys. benzoové z toluenu
Úkol
Navrhni přípravu následujících kyselin a zapiš rovnicemi!
- kyselina propionová
- kyselina ftalová
- kyselina stearová