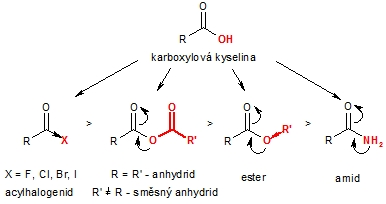
Funkční deriváty karboxylových kyselin
Jsou odvozeny od karboxylových kyselin náhradou H atomu (soli) nebo hydroxylové skupiny OH (halogenidy, estery, amidy); nitrily vznikají náhradou –OH a O.
Přehled funkčních derivátů
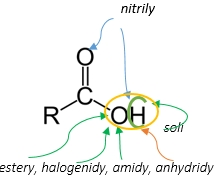
Obr. 1: Odvození funkčních derivátů
-
soli karboxylových kyselin (R-COOMe)
-
estery (R-COOR)
-
amidy (R-CONH2)
-
halogenidy karboxylových kyselin = acylhalogenidy (R-COX)
-
nitrily (R-CN)
-
anhydridy (R-CO-O-CO-R’)
-
imidy (R-CO-NH-CO-R’)
Obr. 2: Schéma vzniku funkčních derivátů (3)
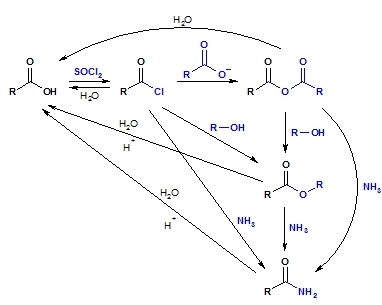
Obr. 3: Vzájemné přeměny funkčních derivátů (3)
Názvosloví
Opisem z názvu karboxylových kyselin, z latinských názvů karboxylových kyselin, triviální.
Soli
Vznikají náhradou atomu vodíku v hydroxylové skupině atomem kovu nebo amonným kationtem; vícesytné kyseliny mohou tvořit i hydrogensoli.
Názvosloví
-
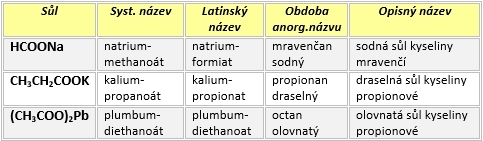
Systematický název je tvořen: latinský název kovu + (di, tri, …) + základ systematického názvu kyseliny + “-oát.”
-
Latinský název: latinský název kovu + základ latinského názvu kyseliny + “-át.”
-
Obdoba anorganického názvosloví: základ triviálního názvu kyseliny + “-an” + název kationtu kovu.
-
Opisný název uvádí název soli a 2. pád kyseliny, z které je sůl odvozena.
Tab. 1: Příklady názvů solí
Příprava solí
Soli se nejčastěji připravují reakcí karboxylové kyseliny s hydroxidem nebo uhličitanem příslušného kovu.
- Neutralizace - reakcí karboxylové kyseliny s hydroxidem:
CH3COOH + NaOH → CH3COONa + H2O
- Reakce karboxylové kyseliny s neušlechtilým kovem, např. zinkem nebo hořčíkem:
2 CH3COOH + Zn → (CH3COO)2Zn + H2
- Reakcí karboxylové kyseliny se solí slabší anorganické kyseliny (uhličitany):
CH3COOH + Na2CO3 → 2 CH3COONa + CO2 + H2O
- Alkalická hydrolýza (zmýdelňování) - sodné a draselné soli vyšších mastných kyselin, zvané mýdla, se připravují zmýdelněním tuků, ve kterých jsou uvedené kyseliny vázané ve formě esterů (průběh reakce viz. estery):
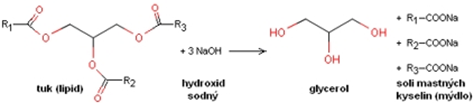
Obr. 4: Zmýdelnění tuků
Reakce solí
-
Dekarboxylace – dochází k odštěpení karboxylové skupiny (CO2) působením silné zásady za zvýšené teploty. Bezvodá sodná sůl karboxylové kyseliny se taví s hydroxidem sodným za vzniku uhlovodíku, který má o jeden uhlík méně než měla výchozí sůl, dále vzniká uhličitan:
RCOONa + NaOH → R- H + Na2CO3
- Vytěsnění kyselin ze solí silnější kyselinou (obvykle anorganickou):
RCOONa + HCl → R- COOH + NaCl
- Hydrolýza solí – karboxylové kyseliny jsou obvykle slabší kyseliny, proto soli podléhají hydrolýze a roztoky mají zpravidla zásaditý charakter:
RCOONa + H2O → R- COOH + Na+ + OH-
Příklady solí a jejich užití
Octan sodný CH3COONa – regulátor kyselosti, v analytice do pufrů, hřejivo („hřející polštářky“).
Octan sodný a draselný CH3COONa, CH3COOK – katalyzátory.
Octan hlinitý - (CH3COO)3Al – v lékařství na otoky.
Octan železitý - (CH3COO)3Fe – barvení látek.
Octan chromitý - (CH3COO)3Cr – barvení látek.
Šťavelan sodný (COONa)2 – v analytice jako základní látka.
Benzoan sodný – C6H5COONa – konzervační prostředek.
Směs palmitanu sodného CH3(CH2)14COONa a stearanu sodného CH3(CH2)16COONa tvoří hlavní část mýdel.
Zdroje
- HUSÁREK, Josef. Wikipedia.cz [online]. [cit. 14.7.2014]. Dostupné z: http://ucitelchemie.upol.cz/materialy/studijni_texty/vyukova_temata/plasty.ppt
- WIKIPEDIA.ORG. [online]. [cit. 6.7. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Deriv%C3%A1ty_karboxylov%C3%BDch_kyselin
- WIKIPEDIA.ORG/. Soli karboxylových kyselin [online]. [cit. 5.7. 2014]. Dostupné z: http://cs.wikipedia.org/wiki/Soli_karboxylov%C3%BDch_kyselin
Obrázky
- Obr. 1: Archiv autora
- Obr. 2: VÍCHA, Robert. WIKI.MEDIK.CZ. [online]. [cit. 29.10.2014]. Dostupné z: http://www.chemie.utb.cz/rvicha/SOC/supportfiles/DOCS/karb_kyseliny_fc_der.doc
- Obr. 3: VÍCHA, Robert. WIKI.MEDIK.CZ. [online]. [cit. 29.10.2014]. Dostupné z: http://www.chemie.utb.cz/rvicha/SOC/supportfiles/DOCS/karb_kyseliny_fc_der.doc
- Obr. 4: VÍTEK, Antonín. CS.WIKIPEDIA.ORG. Schema zmydělnění tuků [online]. [cit. 29.10.2014]. Dostupné z: http://commons.wikimedia.org/wiki/File:Schema_zm%C3%BDdeln%C4%9Bn%C3%AD_tuk%C5%AF.PNG
- Obr. 5: YOUTUBE.COM. Chemický krápník [online]. [cit. 14.11. 2014]. Dostupné z: http://www.youtube.com/watch?v=LiHW2-pHi4I
- Obr. 6: VRZÁČKOVÁ, Eva. WWW.STUDIUMCHEMIE.CZ. Hořící gel [online]. [cit. 10.7. 2014]. Dostupné z: http://www.studiumchemie.cz/pokus.php?id=142
Praktická ukázka
Hořící gel
Pokus s octanem vápenatým

Obr. 6: Ukázka z videa - hořící gel
Efektní pokus s náhlou změnou skupenství - vhodné pro žáky ZŠ
Kontrolní otázka
Příprava solí
Navrhni a zapiš rovnicí nejvhodnější přípravu následujících solí:
-
šťavelan vápenatý,
-
octan hlinitý,
-
benzoan sodný.
Návod
Připrav si vlastní mýdlo a seznam se s jeho vlastnostmi
Postup: Do kádinky s roztokem loje (10 g) v ethanolu (25cm3) přidejte 25 cm3 40% roztoku hydroxidu sodného. Kádinku zakryjte odpařovací miskou se studenou vodou a opatrně ji zahřívejte na síťce (aby směs nevzkypěla). Po 10 – 15 minutách zahřívání ukončete a do směsi přidejte nasycený roztok chloridu sodného. Po zchladnutí se na povrchu směsi vytvoří vrstva mýdla.
Část připraveného mýdla protřepte s destilovanou vodou ve zkumavce. Pozorujte, zda se tvoří pěna.
Roztok mýdla v destilované vodě rozdělte do 3 zkumavek. Do jedné přidejte 10% roztok vápenaté soli a do druhé 10% roztok hořečnaté soli a do třetí pitnou vodu. Směsi protřepte a pozorujte, zda se tvoří pěna.
K roztoku mýdla přidejte několik kapek fenolftaleinu.
Uveďte svá pozorování a vše zdůvodněte.